
1. 介绍(Introduction)
1. 病理学的数字化转型
在过去的数年里,病理学领域正经历着一场深刻的变革 。这场变革的核心在于全切片成像技术(Whole Slide Imaging, WSI)的广泛采用,它正在逐渐取代传统的生理光学显微镜 。
将微观的病理特征以数字化的形式呈现,不仅是工具的更迭,更开辟了病理诊断的新视野 。数字切片的出现极大地提升了临床工作的灵活性,主要体现在以下几个方面:
· 远程诊断与协作:数字化使得远程主诊工作和电信会诊(Teleconsultation)成为可能,打破了地域限制 。
· 效率与平衡:它有助于优化工作负载的分配与平衡,提升实验室的整体运行效率 。
· 科研与教育:数字平台为中心临床试验审查、虚拟教育、创新研究以及跨机构协作提供了便利 。
2. 人工智能(AI)的切入点
随着 WSI 技术的成熟,计算机视觉和人工智能社区开始注意到这一领域,并提供了诸如深度学习(Deep Learning)算法和图像识别等先进的计算病理学方案 。
特别是人工神经网络(ANNs),得益于深度学习的发展,其性能取得了突飞猛进的进步 。研究人员利用大型图像数据集(如癌症基因组图谱 TCGA 或 ImageNet)训练出了各种多样的深度架构 。这些算法展现了令人印象深刻的对象识别能力,并帮助人类在生物医学信息学领域取得了许多新发现 。
3. 未来的焦点:协作还是取代?
随着 AI 在计算机视觉应用中的持续成功,许多研究人员和医生对 AI 抱有极高的期望,认为它能够协助完成数字病理中的多项任务 。
然而,一个极具挑衅性的议题也随之浮现:AI 最终会取代病理学家吗?或者,它如何才能最好地辅助病理学家工作? 。虽然 AI 的潜力巨大且触手可及,但在我们真正利用其潜能之前,仍然有许多来自工程学和病理学视角的严峻挑战需要被克服 。
2. 挑战(Challenges)
虽然 AI 在实验室中表现惊人,但要真正走进病理医生的日常工作流,还面临着从工程到伦理的多重障碍 。
1. 高质量标注数据的匮乏 (Lack of labeled data)
大多数 AI 算法(特别是深度学习)都是“数据饕餮”,需要海量且高质量的标注图像进行训练 。
· 标注成本极高:理想的标注必须由病理专家完成,这不仅意味着高昂的经济投入,还面临专家时间匮乏的瓶颈 。
· 众包的质量隐患:虽然众包标注更便宜快捷,但容易引入噪声,影响模型准确性 。
· 任务枯燥繁琐:对大量图像进行精细标注是一项极其单调的工作,且在图像模糊或网络延迟时尤为困难 。
2. 组织形态的普遍变异性 (Pervasive variability)
人体组织虽然只分为上皮、结缔、神经和肌肉四大类,但从计算角度看,其衍生的模式几乎是无限的 。这种极端的多态性使得算法理解组织架构变得异常困难,模型需要为每一种细微的变异准备大量的训练案例 。
3. 非布尔值的诊断本质 (Non-boolean nature of diagnostic tasks)
目前的论文大多将诊断简化为“是/否”(良性/恶性)的二元分类问题,但这严重简化了临床现实 。
· 复杂的临床决策:真实的诊断包含临床背景理解、认知、感知和经验积累 。
· 谨慎的措辞:面对疑难病例,病理专家常使用描述性或谨慎的术语,而 AI 的强行分类可能无法反映这种不确定性 。
4. 维度障碍 (Dimensionality obstacle)
数字病理图像(WSI)通常是十亿像素(Gigapixel)级别的,尺寸经常超过 50,000 x 50,000 像素 。然而,深度神经网络(ANN)通常只能处理极小的尺寸(如 350 x 350 像素) 。
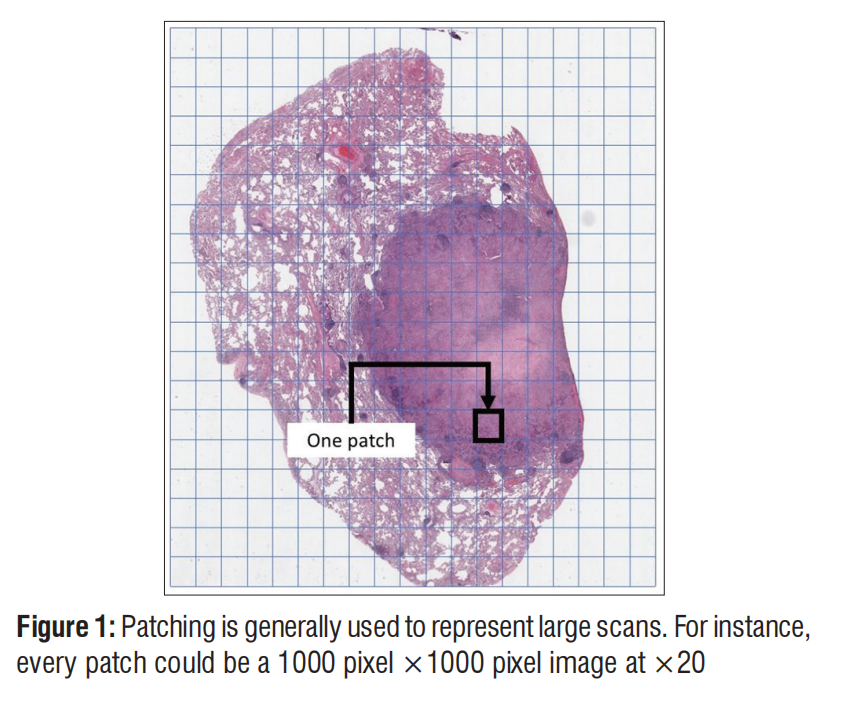
5. 图灵测试困境 (Turing test dilemma)
根据图灵测试的逻辑,机器智能的终极验证是人类的评估 。在数字病理中,病理学家被视为“金标准”和最终评估者 。因此,完全的自动化不仅目前不可能,从审慎角度看或许也并不可取 。
6. 弱人工智能的单任务导向 (Uni-task orientation of weak AI)
我们目前谈论的 AI 大多属于“弱 AI”,即只能在高强度数据训练后完成特定任务 。
· 缺乏通用性:分割、分类、检索等任务需要分别训练模型 。
· 解剖部位局限:针对胃部的模型可能完全不适用于肝部,这种开发模式对资源的需求是巨大的 。
7. 昂贵的计算开销 (Affordability)
深度学习极度依赖图形处理单元(GPU)进行快速数据处理,依靠普通的 CPU 运行简直慢得无法忍受 。对于已经面临数字化转型财务压力的实验室来说,采购 GPU 集群无疑是雪上加霜 。
8. 对抗攻击:决策的脆弱性 (Adversarial attacks)
深度网络有时会表现得像一个极其复杂的“查找表”,甚至可能被误导 。
· 像素级操纵:只需改动极小比例的像素,就能让高性能网络做出错误判断 。
· 噪声风险:切片中的组织褶皱、碎屑或染色污染是否也会被 AI 误诊为癌症?目前的模型在鲁棒性方面仍有待验证 。
9. 缺乏透明度与可解释性 (Lack of transparency)
这是 AI 著名的“黑盒”问题 。深度网络内部数以百万计的计算步骤无法提供一个可被人类理解的决策路径 。在医学界,这种不可解释性是难以接受的,医生必须知道“为什么”才能做出最终诊断并获取监管机构的批准 。
10. AI 的现实主义:落地难 (Realism of AI)
AI 在医疗中的失败案例往往不是技术不行,而是由于部署困难 。病理学家的认可取决于三大关键:
· 易用性:工作流是否简单,输出是否通用易懂 。
· 投资回报率:应用是否能带来经济回报 。
· 信任:是否有确凿的证据证明其性能稳定 。
3. 机遇(Opportunities)
面对标注数据短缺、计算成本高昂等问题,新的技术路径正在重新定义人工智能与病理学的结合方式。
1. 深度特征与预训练 (Pretraining is better)
迁移学习 (Transfer Learning) 的兴起为医学影像带来了曙光 。
· 知识迁移:研究者可以先用数百万张自然图像(如动物、建筑)训练网络,再将其获得的特征提取能力应用到病理图像中 。
· 降低门槛:这种方法只需少量的医学图像进行微调,就能避免从零开始训练的巨大资源消耗,有效缓解了数据匮乏的难题 。
2. 手工特征 (Handcrafted features)
在深度学习大热的今天,传统的计算机视觉方法不应被遗忘 。
· 可解释性强:诸如核大小、腺体形状等“手工特征”是人类可以理解和验证的,这与病理学家的临床经验高度契合 。
· 低能耗:这些特征的提取不需要昂贵的 GPU 集群,在某些场景下的表现甚至能与深度学习并驾齐驱 。
3. 生成式框架 (Generative frameworks)
不同于只做“对错判断”的判别模型,生成模型(如 GANs)专注于理解数据的本质 。
· 深度理解:如果算法能模拟生成一张病理图,说明它已经真正掌握了图像的统计特征 。
· 减少依赖:这类模型在肺部疾病分类等领域已展现潜力,有助于在标签稀缺的情况下进行特征学习 。
4. 无监督学习 (Unsupervised learning)
如果说标注是瓶颈,那么无监督学习就是突破口 。
· 挖掘潜能:利用自组织映射(SOM)或层次聚类等传统 AI 手段,算法可以自动从海量切片中提取有价值的特征 。
· 临床契合:病理医生的日常工作中并不包含大量标注,因此这种无需人工干预的特征提取模式更具实操价值 。
5. 虚拟同行评审 (Virtual peer review)
AI 不应取代医生决策,而应成为医生的“智能图书馆” 。
· 相似病例检索:当医生遇到疑难病例时,AI 可以迅速从全球数据库中找回特征相似的已确诊案例供参考 。
· 质量保证:例如将当前的活检诊断与患者过往的样本进行自动比对,辅助实时质控 。
6. 自动化 (Automation)
AI 擅长处理那些让医生疲劳且枯燥的重复性任务 。
· 繁琐任务代劳:例如自动计算核分裂象(Mitoses)计数、筛查易识别的癌症类型等 。
· 病例分流:AI 可以预先识别高危病例并进行优先级排序(Triage),确保需要紧急关注的切片最先出现在医生桌上 。
7. H&E 图像的“重生” (Re-birth of the H&E image)
传统的苏木精-伊红(H&E)染色图像在 AI 的加持下焕发了第二春 。
· 挖掘深层信息:AI 能够分析单个像素间的微观关系,解锁隐藏在切片中的肿瘤微环境、免疫反应等预后信息 。
· 替代复杂测试:通过常规 H&E 切片预测 Gleason 评分或分子分型,可能减少对昂贵分子测试的依赖 。
8. 让数据科学触手可及 (Making data science accessible)
AI 的最终目标是提升病理学家的职业价值 。
· 价值重塑:通过分析大数据,病理学家将从单纯的“看图者”转变为整合诊断信息的“信息专家”,提高诊断准确性度和个人职业成就感 。
4. 总结(Summary)
通过对这篇论文的深入分析,我们可以清晰地看到,人工智能在数字病理领域的应用正处于一个“希望与挑战并存”的十字路口 。
1. 监管与审批:信任的基石
AI 工具在临床实践中的广泛采用,很大程度上取决于监管机构的批准 。
· FDA 的先行尝试:美国食品药品监督管理局(FDA)已经批准了放射科和眼科领域的 AI 应用,这为病理学提供了宝贵的参考 。
· 降低责任与负担:获得 FDA 批准不仅能为医生提供信心,减少个人执业责任风险,还能增加获得医疗保险报销的机会,并减轻实验室自我验证的负担 。
· 开发者的挑战:为了通过审查,模型开发者需要提供更加详尽的技术决策文档,这无疑会增加研发成本 。
2. 警惕“过度承诺”的风险
AI 社区曾经历过数次因为承诺未能兑现而导致的低谷(即“AI 寒冬”) 。目前,过度吹嘘 AI 能力的危险依然存在 。
· 管理预期:我们必须清醒地认识到,AI 在病理学中的应用不会像当前的狂热所暗示的那样一帆风顺 。
· 稳步前行:只有妥善管理其优势并正视其缺陷,AI 才能在医疗影像和数字病理中实现真正的突破 。
3. 病理学家的核心地位
论文反复强调,病理学家的参与是 AI 成功的关键 。
· 从研发开始:为了确保 AI 软件能真正填补临床空白而不干扰工作流,必须从算法开发阶段就引入病理医生的反馈 。
· 角色的演变:AI 将改变病理学家的职业角色,通过分析大数据来提高其效率、准确性和个人满意度,而非单纯的替代 。
结语
正如论文所述,我们正站在病理学转型的门槛上 。虽然目前还没有大规模商业化的 AI 驱动病理软件工具 ,但通过合理的管理和技术创新,人工智能终将成为病理学家手中不可或缺的利器 。
